Асептический некроз медиального мыщелка бедренной кости лечение. Деформирующий артроз голеностопного сустава. Остеохондропатии таранной кости по типу асептического некроза.
Надпяточная кость, она же таранная – это одна из костей, которая формирует нижний отдел голеностопа, асептический таранной кости грозит пациенту инвалидностью и ограничением подвижности.
Таранная кость покрывается суставным хрящом на шестьдесят процентов. Основной ее функцией является передача массы тела на поверхность стопы: ладьевидную, пяточную и кубовидную кости. Таранную кость можно поделить на три части: блок, головку и задний отросток.
Вследствие особенностей кровотока, в ней может развиться некроз тканей. Если не будет своевременного лечения, заболевание может даже привести человека к инвалидности. Перелом данной кости приводит к осложнению в системе кровообращения. Такое нарушение приводит к некрозу в определенных частях кости, а при затягивании с лечением на ранних стадиях, поражает всю кость. Наиболее чаще асептический некроз возникает у мотоциклистов и спортсменов - прыгунов с большой высоты.
Причины возникновения заболевания
Асептический некроз, он же аваскулярный, может возникнуть при нарушении сосудистого кровотока, который насыщает головку кости. Вследствие такого нарушения возникает аваскулярный некроз в отдельных участках кости, а именно в костном мозге у головки. Это можно сравнить с инфарктом.
При занятиях спортом, в которых происходит упор шейки данной кости на передний край большеберцовой кости, данный упор ведет к смещению или вывиху. Интенсивное подошвенное сгибание так же ведет к смещениям и переломам.
Стадии развития
Некроз по уровню поражения подразделяется на:
- Полный. Особенностями такого заболевания, является частичное или полное омертвление кости.
- Локализационный. Отличием данного вида болезни является поверхностное повреждение. В этом случае некротизируется только внешняя поверхность кости.
- Глубокой. В этом случае происходит омертвение самых глубинных слоев тканей.
Так же в медицине определяются четыре стадии заболевания:
- I стадия. Болезнь не влияет на ограничения движения, только периодически будут возникать боли. Кость в этой стадии поражается на 10%.
- II стадия. В ней некроз ограничивает подвижность из-за сильных болей. В этой стадии наблюдаются трещины.
- III стадия. Сильно уменьшается подвижность из-за сильных и постоянных болей. Ткани кости поражены от 30 до 50%.
- IV стадия. При этой стадии проводят удаление участка омертвевшей кости пострадавшего. Происходит полное разрушение тканей.
Симптомы
Некроз кости таранной, явление довольно частое. Подвергаются ему в основном мужчины, до 8 раз реже женщины. В отличие от , асептический некроз, в основном поражает людей возрастом от 20 до 45 лет. От данного заболевания, одна нога страдает в 60% случаев, а сразу обе в 40%.
Симптомы такого заболевания почти аналогичны симптомам артроза у тазобедренного сустава. Отличить эти две болезни очень сложно. Но нет ничего невозможного. Артроз развивается крайне медленно, а некроз развивается в очень быстрых темпах, буквально за считанные дни.
В большинстве случаев, боль усилиться до предела за первые двое или трое суток.
Диагностика
Как и в любой болезни, успех лечения заключается в своевременном выявлении заболевания. Спасти сустав без хирургического вмешательства, возможно только при обнаружении болезни на ранних стадиях и осуществлении качественного лечения. Главной проблемой является обнаружение некроза, так как на ранних стадиях его довольно сложно диагностировать.
Схожие симптомы с артрозом будут тому причиной. При появлении первых подозрений, врач обычно отправляет пациента на рентгеновское обследование, а оно не в состоянии обнаружить некроз на ранних стадиях. На рентгеновских снимках можно выявить разрушения только на второй или третей стадиях заболевания. Поэтому лечащий врач, который будет руководствоваться только рентгеновским снимком, может упустить возможность пациента выздороветь, не прибегая к хирургическому вмешательству.
Вовремя выявить некроз кости, возможно, только с помощью двух томографий. Помогут распознать болезнь в самом начале, магнитно-резонансное и компьютерное обследование. Именно подобные методики помогут своевременно выявить болезнь и избежать хирургической операции.
Лечение некроза
Сегодня современная медицина разработала ряд препаратов, которые оказывают эффективное воздействие на воспаления и опухоли в процессе лечения некроза таранной кости. Они значительно уменьшают страдание подвергшихся данной болезни и улучшают кровообращение, микроциркуляцию, стимулируют регенерирующие свойства и восстанавливать плотность клеток костной ткани.
Основные усилия при лечении некроза костей, направлены на предотвращение дальнейшего разрушения и восстановление функции кости, а так же на то, что бы уменьшить страдания больного.
Важно не терпеть боль и надеяться на то, что она пройдет, а своевременно обращаться к доктору. И тогда будет возможность быстро и без оперативного вмешательства восстановить функции сустава.
Асептический некроз костей был впервые выявлен у детей и подростков при дифференциальной диагностике с распространенным в то время костно-суставным туберкулезом. Это заболевание отличается от костно-суставной формы туберкулеза гораздо более благоприятным течением. Первое его название - остеохондропатия (буквально «заболевание кости и хряща»). Однако оно не несет информации об этиологии и патогенезе патологических изменений. В мировой литературе этот термин давно не употребляется. Термин «асептические остеонекрозы» указывает как на характер патоморфологических изменений (некроз), так и на неинфекционное происхождение некроза в противоположность, например, остеонекрозам при остеомиелите.
О роли нарушения кровообращения в развитии асептического некроза свидетельствует отсутствие в ранней стадии заболевания проникновения РФП в некротический участок кости при остеосцинтиграфии и усиления его сигнала после контрастирования при МРТ. Несомненно, также значение циркуляторных расстройств в развитии асептического некроза после переломов и вывихов, сопровождающихся разрывами сосудов, а также при гемоглобинопатиях, которые приводят к агрегации эритроцитов и повышению вязкости крови, или при кессонной болезни. Асептический некроз при болезни Гоше и гиперкортицизме объясняют нарушением микроциркуляции вследствие повышения внутрикостного давления. Это происходит из-за разрастания в костномозговых пространствах гистиоцитов при болезни Гоше и из-за увеличения объема жирового костного мозга при гиперкортицизме. Остеонекрозы часто сочетаются с гиперлипидемией. При нарушениях жирового обмена считается возможной жировая эмболия, обусловленная дестабилизацией и агломерацией липопротеинов плазмы крови или разрывами жирового костного мозга и внекостной жировой ткани. Однако явный этиологический фактор выявляется при асептическом некрозе далеко не всегда.
Причины асептического некроза:
- травма (переломы и вывихи);
- гиперкортицизм;
- гемоглобинопатии;
- кессонная болезнь;
- алкоголизм;
- панкреатит;
- коллагенозы (поражение мелких сосудов);
- болезнь Гоше;
- трансплантация почек;
- подагра и гиперурикемия;
- лучевая терапия;
- нарушения жирового обмена;
- сахарный диабет.
Возникновение некроза объясняют ишемией пораженного участка кости. Показано, что уже в первые 12-14 ч после прекращения кровоснабжения гибнут кроветворные клетки, клетки костной ткани могут оставаться жизнеспособными до 2 сут, а клетки жирового костного мозга - от 2 до 5 сут. Однако не все случаи асептического некроза можно объяснить прекращением кровообращения и, как следствие, развитием некроза костной ткани. Часто при асептическом некрозе не удается обнаружить явных причин. В какой форме происходит при этом нарушение кровоснабжения, не ясно. Морфологически сосудистое русло обычно не изменено. Не подвергая сомнению важность гемодинамического фактора, нельзя исключить роль и других факторов в развитии асептического некроза, в том числе повышенной нагрузки. При нарушениях жирового обмена развитию асептического некроза может способствовать статическая перегрузка, обусловленная увеличением веса. Примером могут быть женщины с послеродовым ожирением, у которых вначале возникает асептический некроз головок бедренных костей, а после того, как они начинают пользоваться при ходьбе костылями, - асептический некроз головок плечевых костей. Это можно объяснить переносом нагрузки на руки. Возможно, причина асептического некроза - несоответствие между кровоснабжением данного участка костной ткани и выполняемой нагрузкой.
Эпифизы трубчатых костей и некоторые губчатые кости, поражаемые асептическим некрозом, находятся в относительно неблагоприятных условиях кровоснабжения. Большая часть их поверхности покрыта суставным хрящом, и лишь небольшая часть остается на долю поверхностей, через которые могут проникать сосуды внутрь кости. К тому же в растущем скелете кровоснабжение эпифизов относительно изолировано от остальной сосудистой сети кости, что ограничивает возможность коллатерального кровотока. В этих условиях повышается вероятность кровоснабжения эпифиза или мелкой кости единственной артерией с отсутствием коллатерального кровоснабжения. Асептический некроз развивается, как правило, в головках костей, а не в суставных впадинах. При этом наиболее уязвимой является головка бедренной кости. Асептические некрозы могут иметь множественные локализации. В таких случаях нужно исключить все известные системные причины.
Некрозы, возникающие в метадиафизах длинных костей, принято называть костномозговыми инфарктами, хотя в процесс вовлекается также губчатое вещество. Они имеют гораздо более благоприятное течение, ограничиваются костномозговой полостью, не затрагивают кортикального слоя и обычно выявляются случайно уже в отдаленном периоде после развития инфаркта. Общность происхождения асептического некроза и костномозговых инфарктов подтверждается случаями их сочетания в одной и той же области.
У детей и подростков:
- головка бедренной кости;
- головка II или III плюсневой кости (вторая болезнь Альбана-Келлера);
- ладьевидная кость стопы (первая болезнь Альбана-Келлера);
- эпифизы фаланг пальцев кистей.
У взрослых:
- головка бедренной кости;
- головка плечевой кости;
- блок таранной кости;
- полулунная кость (болезнь Кинбека).
Из числа асептических некрозов исключены варианты оссификации некоторых костей, например пяточной, а также некоторые заболевания, первоначально ошибочно принимавшиеся за асептический некроз. К их числу принадлежит болезнь Шейермана-Мау, рассматривавшаяся как некроз кольцевидных апофизов тел позвонков. Такие некрозы были получены в крайне нефизиологических условиях эксперимента (создание резкого кифоза посредством подшивания хвоста крыс под кожу живота) и никем не подтверждены у человека. В настоящее время преобладает мнение о диспластической природе этого заболевания с расстройством энхондральной оссификации ростковых хрящевых пластинок тел позвонков, неравномерностью роста последних и возникновением локальных выпячиваний в тела позвонков (узлов Шморля). Болезнь Осгуда-Шлаттера возникает в результате микротравматических повреждений, которые происходят у подростков, занимающихся спортом (отрывы мелких хрящевых фрагментов от апофиза бугристости, разрывы волокон самого этого сухожилия, хронический тендинит и бурсит).
Болезнь Кальве характеризуется равномерным уплощением тела позвонка, и в большинстве случаев при ней выявляется эозинофильная гранулема.
Патоморфологически при асептическом некрозе различают несколько зон. Зона собственно некроза характеризуется гибелью всех клеток, в том числе и жировой ткани. Теоретически она должна стать гипоинтенсивной на Т1-взвешенных изображениях при МРТ, однако она может длительно сохранять нормальный для костного мозга сигнал или проявляться другими изменениями сигнала. Имеются указания на возможность длительного сохранения депо липидов и после гибели клеток.
В случае частичного поражения кости, возникают реактивные изменения за пределами зоны некроза. По ее периферии находится зона ишемии, в которой клетки жирового костного мозга могут сохраниться как менее чувствительные к гипоксии. На месте ишемической зоны со временем образуется реактивная зона, отграничивающая некротический участок от живой кости. Некроз вызывает воспалительную реакцию с формированием на границе с некротической зоной грануляционной ткани, рассасывающей некротическую кость. Еще дальше к периферии клетки жирового костного мозга трансформируются в фибробласты или остеобласты, которые продуцируют атипичную волокнистую кость в виде пластов на поверхности некротизированных костных трабекул. За этой зоной располагается зона гиперемии неповрежденной кости.
Остеонекроз не получает прямого отображения на рентгенограммах и выявляется благодаря вторичным реактивным изменениям в окружающей костной ткани.
- Повышенную плотность некротической зоны объясняют ее выключением из обмена, вследствие чего она сохраняет исходную плотность, выделяясь тем самым на остеопеническом фоне, который обусловлен усиленной резорбцией окружающей живой костной ткани в зоне гиперемии.
- Некротический участок отграничивается от неизмененной костной ткани реактивной зоной (если поражается не вся кость, а только ее часть).
Однако, для того чтобы эти вторичные изменения достигли достаточной выраженности и получили отображение на рентгенограммах, должно пройти несколько месяцев. Диагноз может быть гораздо раньше установлен по данным сцинтиграфии («холодная» зона в пораженном отделе кости) и МРТ.
Рассмотренные процессы приводят к ослаблению прочности костных структур. В результате продолжающейся механической нагрузки происходит импрессионный перелом, раньше всего проявляющийся деформацией контура суставной поверхности.
Поскольку суставной хрящ получает питание из суставной синовиальной жидкости, ишемия не повреждает его: в отличие от артрозов, длительно сохраняется нормальная ширина суставной щели. У детей даже развивается гиперплазия суставного хряща с расширением суставной щели.
В дальнейшем пораженная кость или часть кости подвергаются сплющиванию в направлении наибольшего давления, обычно по оси конечности, и отграничивается от живой костной ткани. Изредка один или несколько фрагментов некротической кости отторгаются, становясь свободными внутрисуставными телами. Отграничение некротической кости характеризуется развитием грануляционной ткани на границе с зоной некроза и остеосклероза по периферии. Это отображается на рентгенограмме как двойная кайма по периферии участка остеонекроза. На рентгенограммах отмечаются внутренняя кайма просветления и наружная кайма уплотнения, в некоторых случаях наблюдается только остеосклеротическая кайма. На Т2-взвешенных изображениях МРТ внутренняя кайма имеет повышенную интенсивность сигнала, а наружная - низкую. На Т1-взвешенных изображениях обе зоны выглядят как единая кайма с низким сигналом. Следует учитывать, что такая кайма при МРТ может возникнуть из-за эффекта химического сдвига (особенно при импульсных последовательностях GRE).
Рассмотренная последовательность событий типична для асептического некроза головки бедренной кости и с теми или иными вариантами наблюдается при других локализациях остеонекроза.
На более ранних этапах течения асептический некроз костей проходит одни и те же стадии (некроза, импрессионного перелома, сплющивания) независимо от возраста пациента. В дальнейшем течение асептического некроза отличается в несозревшем и в созревшем скелете. У детей асептический некроз завершается восстановлением костной ткани. Это возможно при реваскуляризации пораженного участка кости, которая происходит в процессе врастания в него соединительной ткани. По-видимому, играют роль также регенераторные потенции хряща в этом возрасте, который подвергается гиперплазии и также врастает в пораженный участок. В исходе заболевания кость остается деформированной, однако структура ее восстанавливается полностью или почти полностью. Такое течение асептического некроза у детей послужило основанием для выделения ряда стадий, отражающих врастание хряща и соединительной ткани в некротическую кость и репаративные процессы в классической схеме Аксгаузена. У взрослых регенеративная способность хряща утрачена или резко ослаблена: восстановление костной ткани не происходит, а процесс рассасывания некротической кости затягивается на годы, завершаясь тяжелым артрозом с дефектом пораженной кости. Именно поэтому у взрослых не может быть той стадийности развития асептического некроза, которая отражена в схеме Аксгаузена.
Особая форма поражения субхондральных отделов костей - ограниченный асептический некроз, который занимает часть суставной поверхности. Степень распространения асептических некрозов различна - от тотального поражения субхондрального отдела кости, мелкой кости запястья или предплюсны до изменений, ограничивающихся небольшими участками. При этом ограниченные асептические некрозы отличаются определенным своеобразием и рассматриваются как особая форма. С другой стороны, рассекающий остеохондроз Кенига, рассматривавшийся ранее как ограниченный асептический некроз, имеет травматическое происхождение.
Выделяют 3 группы асептических некрозов:
- распространенные асептические некрозы в незрелом скелете;
- распространенные асептические некрозы в зрелом скелете;
- ограниченные асептические некрозы.
- Плаксейчук Ю.А.
- Салихов Р.З.
- Соловьев В.В.
Ключевые слова
АСЕПТИЧЕСКИЙ НЕКРОЗ / ОСТЕОНЕКРОЗ ТАРАННОЙ КОСТИ / АРТРОДЕЗ ГОЛЕНОСТОПНОГО И ПОДТАРАННОГО СУСТАВОВАннотация научной статьи по медицине и здравоохранению, автор научной работы - Плаксейчук Ю. А., Салихов Р. З., Соловьев В. В.
Авторы наблюдали 28 пациентов с асептическим некрозом таранной кости. У 5 пациентов с переломом таранной кости аваскулярный некроз был выявлен на ранней стадии, проведено консервативное лечение с полным восстановлением. 23 пациентам понадобилось оперативное вмешательство: двухсуставный артродез. Среди оперированных больных сращение достигнуто у 22 пациентов (95,6%). Клинический результат был отличным у 6 больных (26,1%), хорошим у 12 пациентов (52,2%), удовлетворительным у 3 пациентов (13%) и плохим у 2 пациентов (8,7%). Осложнения были у 4 пациентов. Предложен новый способ двухсуставного артродеза надтаранного и подтаранного сустава с костной пластикой за счет остеотомированной малоберцовой кости с компрессией в аппарате Илизарова. По предложенному способу прооперировано 15 больных.
Похожие темы научных работ по медицине и здравоохранению, автор научной работы - Плаксейчук Ю.А., Салихов Р.З., Соловьев В.В.,
-
Хирургическое лечение больных с артрозом голеностопного сустава
2012 / Плаксейчук Юрий Антонович, Салихов Рамиль Заудатович, Соловьёв Владислав Всеволодович -
Остеонекроз головки бедренной кости после травматического вывиха, полученного в результате дорожно-транспортного происшествия
2011 / Лебедев Виктор Федорович, Виноградов Валентин Георгиевич, Редков Сергей Николаевич, Сонголов Геннадий Игнатьевич, Галеева Ольга Павловна, Дмитриева Людмила Аркадьевна, Андаева Татьяна Михайловна, Федорец Сергей Степанович -
Внешняя фиксация переломов таранной кости
2012 / Павлишен Ю. И. -
Чрескостный остеосинтез в лечении сложных переломов таранной кости
2011 / Климовицкий В. Г., Антонов А. А., Лавриненко О. В., Черныш В. Ю., Лобко А. Я. -
Роль остеосцинтиграфии и рентгенографии у пациентов с остеонекрозом при эндопротезировании коленных суставов
2016 / Король П.А., Ткаченко М.Н., Бондар В.К.
Текст научной работы на тему «Современные методы лечения аваскулярного некроза таранной кости и их результаты»
Ю.А. ПЛАКСЕЙЧУК, Р.З. САЛИХОВ, В.В. СОЛОВЬЕВ УДК 616-718-71
Республиканская клиническая больница Министерства здравоохранения Республики Татарстан
Современные методы лечения аваскулярного некроза таранной кости и их результаты
I Салихов Рамиль Заудатович
врач, травматолог-ортопед отделения ортопедии, научный сотрудник
420140, г. Казань, ул. Ноксинский Спуск, д. 26, кв. 194, тел. 8-917-286-40-34, е-таН; [email protected]
Авторы наблюдали 28 пациентов с асептическим некрозом таранной кости. У 5 пациентов с переломом таранной кости аваскулярный некроз был выявлен на ранней стадии, проведено консервативное лечение с полным восстановлением. 23 пациентам понадобилось оперативное вмешательство: двухсуставный артродез. Среди оперированных больных сращение достигнуто у 22 пациентов (95,6%). Клинический результат был отличным у 6 больных (26,1%), хорошим у 12 пациентов (52,2%), удовлетворительным у 3 пациентов (13%) и плохим у 2 пациентов (8,7%). Осложнения были у 4 пациентов. Предложен новый способ двухсуставного артродеза надтаранного и подтаранного сустава с костной пластикой за счет остеотомированной малоберцовой кости с компрессией в аппарате Илизарова. По предложенному способу прооперировано 15 больных.
Ключевые слова: асептический некроз, остеонекроз таранной кости, артродез голеностопного и подтаранного суставов.
J.A. PLAKSEYCHUK, R.Z. SALIKHOV, V.V. SOLOVYEV
Republican Clinical Hospital of Ministry of Health Care of the Republic of Tatarstan
Modern methods of treatment of avascular necrosis of the talus and their results
The authors observed 28 patients with aseptic necrosis of the talus. In 5 patients with a fracture of the talus avascular necrosis was identified at an early stage, conservative treatment is carried out with full recovery. 23 patients needed surgery: biarticular arthrodesis. Among the operated patients achieved fusion in 22 patients (95.6%). The clinical outcome was excellent in 6 patients (26.1%), good in 12 patients (52.2%), satisfactory in 3 patients (13%) and poor in 2 patients (8.7%). Complications were 4 patients. A new method of biarticular arthrodesis of overtalus and subtalus joint with bone plastic for account of osteotomic fibula with compression in the Ilizarov apparatus was proposed. According to the proposed method 15 patients underwent surgery.
Keywords: aseptic necrosis, osteonecrosis of the talus, ankle arthrodesis and subtalar joints.
Таранная кость - вторая по размерам кость предплюсны и имеет уникальную канальную структуру для распределения веса тела. Приблизительно 60% поверхности ее покрыто хрящом и ни одна мышца или сухожилие не прикрепляются к ней. Следовательно, только ограниченная область проницаемой кости доступна для сосудистой перфорации. Эта особенность в комбинации с малым диаметром питающих сосудов, вариацией внутрикостных анастомозов и недостатком коллатерального кровоснабжения являются предрасполагающими факторами к развитию остеонекроза таранной кости при нарушении ее кровоснабжения. Аваскулярный некроз - это гибель кости в результате ишемии. Асептический некроз таранной кости происходит при прекращении кровоснабжения в любой ча-
сти сосудистого русла, включая артерии, капилляры, синусоиды, вены. Оно может наступить в результате обструкции, компрессии, разрыва сосудов. Во всех случаях ишемический некроз кости происходит из-за недостатка обеспечения кровью, и последующего кислородного голодания. Ответ организма на остеонекроз попытка восстановления путем реоссификации, реваскуляризации и резорбции некротической кости. При наличии этих процессов аваскулярный некроз кости визуализируется рентгенологически .
Развитие аваскулярного некроза часто связано с травмой - переломом таранной кости, полным вывихом, при которых происходит повреждение питающего сосуда. Асептический некроз таранной кости, по данным разных авторов, составляет от 60 до
80% осложнений переломов таранной кости, сопровождаемых вывихами в голеностопном и подтаранном суставах. В практике встречаются случаи развития аваскулярного некроза на поздних сроках после травмы, обычно при наличии сопутствующих факторов: злоупотребление алкоголем, курение, при сосудистой патологии и избыточном весе, при приеме глюкокортикостероидов. По степени поражения асептический некроз может захватывать весь блок таранной кости или фрагмент отломка в зоне «выпадения» питающего сосуда. В зависимости от размера очага, а также от срока развития тактика лечения может меняться. Немаловажную роль при этом играет своевременное выявление асептического некроза таранной кости. В данном исследовании мы попытались обобщить вопросы диагностики и лечения аваскулярного некроза таранной кости в зависимости от стадии процесса и размера очага поражения.
Цель исследования - улучшить результаты лечения пациентов с аваскулярным некрозом таранной кости.
Материалы и методы
Проведена оценка результатов лечения 28 пациентов с асептическим некрозом таранной кости и отдаленных результатов до 5 лет. У 15 пациентов асептический некроз развился после перелома таранной кости, у 13 - на отдаленных сроках после травмы области голеностопного сустава. Интервал между травмой и появлением признаков асептического некроза таранной кости составил от 4 месяцев до 8 лет. Для анализа больных с переломом таранной кости использовали классификацию переломов таранной кости Нашк1пэ-Сапа!е: тип 1 - без смещения, тип 2 - со смещением и подвывихом в подтаранном суставе, тип 3 - с вывихом тела тарана в голеностопном суставе, тип 4 - с вывихом в голеностопном и таранно-ладьевидном суставах. У 5 пациентов асептический некроз был выявлен на ранней стадии (до развития коллапса суставной поверхности) на сроке 4-8 месяцев, подтвержденных данными РКТ у 4 больных и МРТ у 1 больного. На рентгенограммах этих больных обнаруживалась аваскуляризация фрагмента таранной кости, так как он не участвовал в декальцинации, заметной в окружающей кости. Из них 1 пациент имел 1-й тип перелома, у 4 пациентов имелся 2-й тип перелома таранной кости. Сразу после получения травмы всем им было проведено адекватное и своевременное хирургическое лечение с полным восстановлением анатомических взаимоотношений. Проведенное консервативное лечение (длительная разгрузка конечности, сосудистые препараты) позволило получить положительный результат. Последовательные рентгенограммы показали постепенную реваскуляризацию, которая происходила сначала в зоне перелома, а затем распространялась на пораженный участок. Последними реваскуляризировалась субхондральная кость и суставной хрящ голеностопного сустава. Как в голеностопном, так и в подтаранном суставах обнаруживалось сужение суставного пространства. У 10 пациентов с 3-м и 4-м типами переломов таранной кости асептический некроз развился на сроке 4 -24 месяцев, у 8 из них репозиция отломков была неполной. У 7 пациентов процесс располагался в куполе таранной кости, у 3 пациентов - в задненижнем фрагменте таранной кости. Этим больным был выполнен двухсуставный артродез.
В нашей практике мы столкнулись с развитием посттрав-матического аваскулярного некроза таранной кости у 13 больных с повреждениями области голеностопного сустава без перелома таранной кости, причем на разных сроках давности травмы. У 12 из них выявлены предрасполагающие факторы: курение - у 7, злоупотребление алкоголем - у 3, сосудистая
патология - у 4, избыточный вес - у 3, прием глюкокортикостероидов - у 2 больных. Диагноз выставлен на основании клинико-рентгенологических признаков: болевой синдром в области голеностопного сустава, связанный с нагрузкой, ограничение движений в голеностопном и подтаранном суставах, коллапс купола таранной кости с артрозом голеностопного и подтаранного суставов. У 7 из них диагноз подтвержден РКТ, у 3 - МРТ. Оперативное вмешательство было выполнено 23 пациентам (10 пациентов с переломом таранной кости и 13 без него) - двухсуставный артродез (надтаранного и подтаранного суставов) в аппарате Илизарова. Оперированы без применения костной пластики 3 больных. Костный аутотрансплантат из крыла подвздошной кости был использован у 3 больных, местный трансплантат - у 17. Нами предложен способ двухсуставного артродеза надтаранного и подтаранного сустава с костной пластикой за счет остеотомированной малоберцовой кости с сохранением ее связи с мягкими тканями (Патент РФ на изобретение № 2334480 от 27.09.08). Фиксация осуществляется в аппарате внешней фиксации, что позволяет минимизировать травматизацию таранной кости, осуществлять дозированную компрессию. Нагрузку на оперированную конечность начинали с первых дней после операции. Аппарат демонтировали, как правило, через 3 месяца при достижении рентгенологических признаков консолидации. По предложенному способу прооперировано 15 больных.
Результаты
Для оценки эффективности проведенного лечения использованы рентгенологические и клинические признаки. Рентгенологические признаки включали: оценку сращения (трабекуляция через зону перелома или артродеза), механическую ось конечности, наличие артроза прилегающих суставов. Клинический результат (согласно модифицированной шкале для заднего отдела стопы Американского ортопедического общества стопы и голеностопного сустава (АОРАв)) считали отличным, если пациент не имеет никакой боли или ограничения в повседневных и иных действиях, не применяет ортез или другие вспомогательные средства при ходьбе, может пройти больше, чем шесть кварталов (порядка 1500 метров). Результат считали хорошим, если у пациента бывает умеренная боль и имеется ограничение ряда действий (ходьба по неровной поверхности, бег и т.п.), но не повседневной активности, не используется ортез или иные использовать вспомогательные средства при ходьбе, пациент может пройти больше чем шесть кварталов. Результат считали удовлетворительным, если обследуемый имеет частую умеренную боль и имеет ограничение в повседневных действиях и при активном отдыхе, нуждается в индивидуальной обуви или использовании трости и может пройти максимум 4-6 кварталов (1000-1500 метров). Результат считался плохим, если у пациента выраженный болевой синдром, который вызывает серьезное ограничение в повседневной жизни, больной нуждается в использовании ортеза, костылей, или инвалидного кресла и может пройти не более 4 кварталов (менее 1000 метров).
У всех 5 пациентов с 1-м и 2 типами переломов таранной кости после проведенного консервативного лечения получен отличный результат, хотя срок восстановления достигал порядка 2 лет. В группе оперированных больных сращение достигнуто у 22 пациентов (95,6%). Клинический результат был отличным у 6 больных (26,1%), хорошим - у 12 пациентов (52,2%), удовлетворительным - у 3 пациентов (13%) и плохим - у 2 пациентов (8,7%). У 2 пациентов сращение наступило с замедленной консолидацией. У 2 пациентов была спицевая инфекция, купированная местным лечением и приемом антибактериальных препаратов.
Обсуждение
В начальной стадии аваскулярный некроз таранной кости может быть пропущен. Со временем в результате гиперемии начинается резорбция здоровой кости, что приводит к остеопении. Некротизированная кость не может быть резорб-цирована, т.к. имеется нарушение кровоснабжения, что проявляется усилением рентгеноконтрастности по сравнению с окружающей остеопорозной костью. В этот момент асептический некроз кости подтверждается рентгенологически. Непрозрачность некротизированной кости возрастает при происходящей реоссификации и формировании новой кости вокруг некротизированных трабекул. Этот процесс лежит в основе проявления склероза при аваскулярном некрозе таранной кости. В дополнении к реоссификации вокруг некротической кости происходит реваскуляризация и резорбция. Рентгенологически это проявляется ободком вокруг зоны некроза . МРТ является наиболее чувствительным методом обнаружения остеонекроза таранной кости, особенно на ранних стадиях, хотя наличие металлоконструкций может явиться противопоказанием. Кроме того, МРТ может быть использована при подозрении на асептический некроз таранной кости с нормальной рентгенологической картиной. При РКТ также выявляются характерные признаки при остеонекрозе таранной кости, и она должна быть использована для подтверждения рентгенографии. Наше исследование подтвердило высокую значимость этих методов. Тем не менее стандартная рентгенография и внимательность врача остаются основой диагностики и наблюдения динамики ава-скулярного некроза таранной кости. При раннем выявлении асептического некроза таранной кости и отсутствии нарушений анатомических структур возможна регрессия процесса и полное восстановление, хотя для этого требуется длительное лечение. У больных с переломом таранной кости риск сосудистого нарушения и последующего остеонекроза соразмерен с величиной смещения и вывиха при этих повреждениях. По данным литературы , при 1-м типе перелома риск развития аваскулярного некроза составляет 0-15%, при 2-м - риск 20-50%, при 3-м типе перелома риск асептического некроза близок к 100%. При 4-м типе, когда происходит вывих или подвывих в голеностопном, подтаранном, таранно-ладьевидном суставах, риск остеонекроза также составляет 100%. Прогноз зависит также от своевременности и адекватности проводимого лечения, качества репозиции, наличия сопутствующих заболеваний. При развитии аваскулярного некроза на ранних сроках после травмы (до 9-12 мес.), процесс носит обратимый характер. Консервативное лечение (длительная разгрузка сустава, сосудистая терапия, физиолечение) позволяют получить хорошие результаты при условии полного восстановления анатомических взаимоотношений. По нашим данным, процесс принял обратимый характер у пациентов с 1-м и 2-м типами переломов, у больных с 3-м и 4-м типами переломов понадобился артродез. Описанные в литературе варианты хирургического лечения на ранних стадиях (до развития коллапса суставной поверхности) - остеоперфорация таранной кости , применение неваскуляризированного и васкуляризированного костных трансплантатов пока не позволяют достоверно говорить о положительных результатах из-за небольшого количества больных. При асептическом некрозе таранной кости в стадии компрессии происходит разрушение суставной поверхности. Чаще всего поражается суставная поверхность блока, а также нижней суставной поверхности таранной кости. Таранная кость теряет свою трабекулярную структуру и не может обеспечивать распределение нагрузки веса тела между голенью и стопой в процессе ходьбы. Исходом является тяжелый деформирующий артроз
надтаранного и подтаранного суставов. Методом выбора в таком случае является артродез надтаранного и подтаран-ного суставов. Ряд авторов предлагают астрагалэктомию, однако данная процедура имеет ряд существенных отрицательных сторон: она травматична, происходит укорочение конечности порядка 4 см, возникает резкая нагрузка на суставы переднего отдела стопы, что приводит впоследствии к рецидиву болевого синдрома. Мы считаем необходимым сохранение жизнеспособной части таранной кости. Основная проблема артродезирования при асептическом некрозе таранной кости - затруднение при получении костного сращения из-за резко нарушенного кровообращения таранной кости, даже при компрессионном артродезе. Предложены способы артроде-за голеностопного сустава с костной пластикой свободными трансплантатами, например, из крыла подвздошной кости [У] или из передней поверхности нижнего конца б/берцовой кости с фиксацией спицами и иммобилизацией гипсовой повязкой , или с расщеплением наружной лодыжки в сагиттальной плоскости на два фрагмента . Вышеуказанные костнопластические способы являются достаточно травматичными, не позволяют производить дополнительную компрессию, что может привести к несостоятельности артродеза. Известной проблемой артродезирования надтаранного сустава является неплотное прилегание поверхностей таранной кости к суставным поверхностям большеберцовой и малоберцовой костей после удаления суставного хряща. Особенно актуальна данная проблема становится при развитии аваскулярного некроза таранной кости, когда после удаления очага остеонекроза возникает дефицит костной массы . Предложенный нами метод лишен данных недостатков: смещение лодыжки до плотного соприкосновения с большеберцовой, таранной и пяточной костями, с перекрытием артродезируемой области голеностопного и подтаранного суставов, с сохранением связи с малоберцовой костью, за счет косой линии остеотомии, позволяет получить, после сращения единый мощный костный блок. Аппарат внешней фиксации позволяет восстановить ось конечности, осуществить продольную компрессию и раннюю нагрузку. Результаты лечения позволяют рекомендовать предложенную методику хирургического лечения у пациентов с остеонекрозом таранной кости.
У пациентов с переломом таранной кости имеется высокий риск развития аваскулярного некроза таранной кости, что требует настороженности лечащего врача. Остеонекроз таранной кости также может развиться на отдаленных сроках после травмы голеностопного сустава. Для своевременного выявления асептического некроза таранной кости требуется применение МРТ или РКТ, для контроля динамики процесса - рентгенография. При выявлении асептического некроза таранной кости на ранней стадии показано проведение консервативного лечения при условии полного восстановления анатомии таранной кости, отсутствии признаков артроза голеностопного и подтаранного суставов. При развитии асептического некроза таранной кости с импрессией суставной поверхности блока и артрозом голеностопного и подтаранного суставов показан двухсуставный артродез. Предложенная нами методика двухсуставного артродеза с помощью васкуляризированного костного трансплантата из малоберцовой кости в сочетании с продольной и боковой компрессией, достигаемой с помощью аппарата Илизарова, позволяет получить сращение без применения астрагалэктомии. Ранняя нагрузка оперированной конечности (сразу после заживления операционной раны) способствует более быстрой адаптации больного, ускоряет сращение и реабилитационный процесс.
ЛИТЕРАТУРА
1. Christman R.A., Cohen R. Osteonecrosis and osteochondrosis. In: Foot and ankle radiology. St Louis, Mo: Churchill Livingstone, 2003; 452-481.
2. Resnick D., Sweet D.E., Madewell J.E. Osteonecrosis: pathogenesis, diagnostic techniques, specific situations, and complications. In: Diagnosis of bone and joint disorders. 4th ed. Philadelphia, Pa: Saunders, 2002; 3599-3685.
3. Adelaar R.S. The treatment of complex fractures of the talus. Orthop Clin North Am 1989; 20: 691-707.
4. Mont M.A., Schon L.C., Hungerford M.W., Hungerford D.S. Avascular necrosis of the talus treated by core decompression. J Bone Joint Surg Br 1996; 78: 827-30.
5. Horst F. et al. Avascular necrosis of the talus:current treatment options. Foot Ankle Clin N Am 9 (2004): P. 757-773.
6. Hussl H., Sailer R., Daniaux H., Pechlaner S. Revascularization of a partially necrotic talus with a vascularized bone graft from the iliac crest. Arch Orthop Trauma Surg 1989; 108: 27-29.
7. Буачидзе О.Ш., Оноприенко Г.А. Артродез голеностопного сустава // Изобретательство и рационализаторство в медицине. - М., 1981. - С. 116-118.
8. Morris, H.D., Hand W. L. and Dunn A.W. The modified Blair fusion for fractures of the talus. J. Bone and Joint Surg., 53-A: 1289-1297, Oct. 1971. 53-A1289.
9. Данилова А.Е. Сравнительная оценка методов артродеза голеностопного сустава / Данилова А.Е. // В кн.: Вопросы восстановительной хирургии, травматологии, ортопедии. - Т. 9. - 1964. - С. 176.
10. Horst F. et al. Avascular necrosis of the talus: current treatment options // Foot Ankle Clin. N Am. - 2004. - № 9. - P. 757-773.
Асептический некроз - омертвение участка костной ткани в субхондральном отделе суставной поверхности кости, обычно связанное с локальным нарушением кровообращения в определенном участке кости . Заболевание обычно развивается на фоне травмы сустава, применения кортикостероидов, злоупотребления алкоголем, панкреатита, серповидноклеточной анемии, ионизирующей радиации и др. При отсутствии очевидной причины асептический некроз костной ткани (АНКТ) диагноз формулируется как идиопатический некроз кости, но количество таких диагнозов в последнее время уменьшается с расширением возможностей медицины .
Рентгенологическая диагностика позволяет определить поздние стадии заболевания при фрагментации или деформации головки бедренной кости. В большинстве случаев ортопедический прогноз неблагоприятный - тяжелый деформирующий артроз тазобедренного сустава, при котором нередко применяют эндопротезирование, артродез сустава или корригирующие остеотомии как методы выбора хирургического лечения. Ранняя диагностика возможна лишь с применением магнитно-резонансной томографии (МРТ) тазобедренного сустава и дает надежду на благоприятный исход заболевания с применением консервативного или хирургического лечения.
Заболевание наиболее часто отмечается у мужчин (8:1) молодого и среднего возрастов (>⅔ всех случаев) и составляет 1,5–2% всей ортопедической патологии . Наиболее частой причиной нетравматического асептического некроза головки бедренной кости (АНГБК) являются кортикостероидная терапия и злоупотребление алкоголем.
В литературе одинаково широко представлены две точки зрения: травматическая и сосудистая. Известно, что АНКТ может быть вызван различными причинами: нарушением целостности артерий путем их скручивания или сдавления, эмболией, длительным спазмом артерий, венозным стазом и другими механическими воздействиями. АНГБК в результате травмы сустава (вывих, перелом зоны метаэпифиза) или хирургического вмешательства изучен достаточно полно, и механизм его возникновения обусловлен нарушением зоны артериального и венозного кровотока .
Сложнее обстоит вопрос изучения патогенеза при так называемых нетравматических АНГБК. Доказано, что в результате микротравмы, перегрузки сустава и других неблагоприятных факторов в костной ткани происходят процессы «переутомления». Импульсы из очага идут к коре головного мозга и вызывают соответствующие обратные сигналы, вызывающие спазм сосудов или застой крови и лимфы, нарушение обмена веществ, накопление в кости продуктов распада. Это обусловливает изменение физико-химических и структурно-динамических свойств кости, приводящих к медленному разрушению костных балок, дальнейшему затруднению местного кровообращения и прогрессированию процесса. Эта теория «хронической микротравмы» поддерживается и в настоящее время многими исследователями.
В обзоре литературы А.Я. Коробкова (1994) сделан вывод, что все некрозы головки бедра - ишемического происхождения, возникающие в результате эмболии артерий . Согласно сосудистой теории, АНГБК - результат изменения местного кровообращения, в основе которого могут возникнуть прерывание артериального кровообращения или затруднение венозного оттока. Изменение расстройства венозной циркуляции в пораженном диафизе бедра больных асептическим некрозом позволили некоторым авторам высказать предположение, что первичным изменением является венозная недостаточность с последующим переходом процесса на артериальную систему. Вследствие морфологических изменений пути нормального оттока плохо прослеживаются, выявляется более густая венозная сеть, преобладает варикозный тип венозной системы, что позволило констатировать резкое расширение вен, замедленный кровоток и стаз, повышение активности протромбинового индекса, повышение коагуляции и вязкости крови . Нарушения кровотока проявляются повышением кровяного внутрикостного давления, что усугубляет ишемические нарушения. Одной из причин остеонекроза головки бедра является повышение внутрикостного давления в проксимальном конце бедра.
Головка бедра представляет собой закрытый отсек и поэтому кость очень чувствительна к любым ишемическим колебаниям. На фоне повышенного внутрикостного давления происходит тромбоз сосудов, ишемия прогрессирует, что приводит к некрозу костных балок. Разрушение кости в дальнейшем наступает там, где больше выражена ишемия и нагрузка на головку бедра. По мнению Г.С. Кильчевского (1963) анальгетики и противовоспалительные лекарства, а также алкоголь ведут к охранению от боли и снятию воспалительного состояния . Это сочетается с остеонекрозом и перегрузкой определенной области головки бедренной кости, что приводит к разрушению субхондральной кости и локальному остеопорозу. Экспериментальными исследованиями, сопоставленными с гистологическим изучением операционного материла, показано, что при нарушении кровотока в зоне эпифиза на 3–5-е сутки образуются очаги остеонекроза, которые в процессе реваскуляризации замещаются остеогенной тканью и в процессе дифференцировки трансформируются в нормальную костную ткань. При неблагоприятных условиях (перегрузка сустава) на границе участка остеонекроза и окружающими тканями развиваются перифокальная зона фиброза, а затем на фоне вторичных циркуляторных нарушений формируется order essay зона перифокального костного склероза. Гистологически в этот период костные балки лишены остеоцитов, пространства между ними заполнены белковыми массами, участок остеонекроза отграничен фиброзной тканью. Происходит сминание зоны остеонекроза, сопровождающееся переломами субхондральной костной пластинки с отслойкой суставного хряща от зоны остеонекроза с локальным механическим его повреждением, дегенерацией и отслоением. На более поздних стадиях в зоне реактивных изменений и в области очага остеонекроза формируется замыкающая костная пластинка, кистовидная перестройка и другие характерные для деформирующего артроза изменения.
Сегментарное поражение верхнепереднего участка головки бедра поддерживается статической нагрузкой этой области. Деструкция суставного хряща приводит к развитию синовита (реактивного артрита) тазобедренного сустава . При измерении ширины суставной щели установлено, что в среднем она составляет 5,1 мм с разницей между правым и левым суставом не более 0,3 мм. Увеличение этих показателей >7 и >1 мм (соответственно) указывает на синовит тазобедренного сустава.
Общая причина, объединяющая все нетравматические случаи остеонекроза - остеопения. При этом в передневерхнем участке головки бедра, на который приходится бо`льшая часть нагрузки, происходит перелом от «утомления» остеопенических трабекул. Предполагается, что аккумуляция сломанных трабекул может привести к закрытию потока артериальной крови и вызвать некроз кости.
Комбинация остеопороза, механического давления, лекарственных средств, воспаления и боли приводят к субхондральному трабекулярному перелому и последующему разрушению и дегенеративному артриту тазобедренного сустава. У всех пациентов резко выражены нарушения функции передвижения, обусловленные болевым синдромом, ограничением движений в суставе, гипотрофией и нарушением функции мышц.
АНКТ при ревматических заболеваниях привлекают особое внимание и являются одной из актуальных проблем современной ревматологии в связи с явным учащением этой костной патологии, неясностью механизмов развития, неуклонно прогрессирующим течением и сложностью лечения.
Данная проблема очень важна в практике врача-ревматолога, поскольку эти осложнения отмечаются в 10–70% случаев при ревматоидном артрите (РА), системной красной волчанке (СКВ), системной склеродермии, анкилозирующем спондилоартрите и др. (Насонов Е.Л., 2002) . В основе сосудистой теории остеонекроза костей, получившей наибольшее распространение, лежит васкулит. Васкулит при РА, СКВ представляет собой воспаление сосудов, вызванное отложением иммунных комплексов в субэндотелиальном слое базальной мембраны костных сосудов. При этом нарушается кровообращение в головке бедренной кости и вертлужной впадине. АНКТ при СКВ чаще всего связаны с нарушением кровоснабжения участка кости. Наиболее тяжелые из них - это последствия в результате АНГБК и височно-нижнечелюстного сустава. К сожалению, именно он и отмечается наиболее часто. В литературе также имеются сообщенияоб асептическом некрозе головок плечевых костей, наблюдавшемся у больных люпус-нефритом, а также у пациентов без поражения почек. Также АНКТ может возникать как в период приема лечебной дозы преднизолона (30 мг/сут), так и в период ремиссии процесса, на фоне минимальной поддерживающей стероидной терапии. Патогенез этого тяжелого осложнения связывается как с длительной стероидной терапией, так и с поражением микроциркуляторного русла, свойственным вообще СКВ .
Нарушения в системе микроциркуляции имеют генерализованный характер и считаются одними из важных факторов патогенеза РА и его осложнения как на уровне собственной сосудистой стенки, так и внутри сосудов. Они ответственны за уменьшение тканевого и регионарного кровотока с последующими изменениями в структуре и функции органа и ткани. Нормальный обмен веществ и функционирование любого органа невозможны без адекватного состояния микроциркуляции. При этом любой патологический процесс происходит с изменениями микроциркуляторного русла и может варьировать от локальных (периферическая ишемическая полинейропатия, дигитальный артериит, синдром Рейно, сетчатое ливедо и др.) до собственно системных васкулитов (легочного, коронарного, мезентериального и церебрального) и в основе своей имеет аутоиммунный генез.
На начальных этапах заболевания нарушаются реологические свойства крови в системе микроциркуляции. Сосудистый спазм в сочетании с измененными реологическими свойствами замедляет ток крови и ведет к извращению условии транскапиллярного обмена в очаге некроза. Нарушение кровообращения в головке бедренной кости приводит к снижению ее механической прочности, повышая вероятность деформации головки бедра.
Ряд исследователей полагают, что в случае нарушения кровообращения прежде всего поражается хрящ, который при этом теряет свои эластические свойства, а затем процесс переходит на субхондральный слой головки бедренной кости и вертлужную впадину.
В основе теории развития остеонекроза кости лежит функциональная перегрузка тазобедренного сустава или его биологическая неполноценность, важным предрасполагающим фактором которой является остеопороз.
Ряд авторов считают причиной развития АНГБК резкое повышение внутрикостного давления, вызванного спастическими перегрузками. При этом повышается контактное давление на участки суставной поверхности хряща и наступает его дезорганизация. Хрящ теряет способность переносить давление и растяжение, что приводит к его деструкции .
Отдельного внимания заслуживает выявление связи между приемом глюкокортикостероидов (ГКС) и развитием остеонекроза костей, в том числе и АНГБК. Этот вопрос обсуждается во многих исследованиях. Более того, некоторые исследователи сообщают о четкой зависимости развития АНГБК от дозировки ГКС. Одни авторы считают единственным достоверным фактором риска высокую суточную дозу ГКС, другие, напротив, не выявили прямой зависимости развития АНГБК от средней суточной дозы, как в 1-й месяц приема ГКС, так и впервые 3; 6 и12 мес стероидной терапий. Однако некоторые авторы отмечают развитие остеонекроза у больных РА и СКВ, никогда не получавших ГКС. Подобные случаи являются крайне редкими. Как правило, развитию АНГБК при ревматоидном заболевании предшествует гормональная терапия. Для сопоставления больных СКВ с АНГБК и без него по активности болезни не удалось выявить различий между этими двумя группами.
Для объяснения возникновения АНГБК при ревматоидном заболевании необходимо было выяснить возможную связь остеонекроза костей с действием ГКС на жировой обмен, ведущий к повышению липидов крови, и последующей жировой эмболией артерии головки бедра. Этим объясняется и повышение внутрикостного давления, препятствующего нормальному кровообращению в этом районе.
В развитии патологии тазобедренного сустава участвуют все его компоненты. Воспалительно-дегенеративные поражения мышечно-связочного аппарата, несущего наибольшую нагрузку, проявляются болью и обусловливают развитие сгибательных контрактур. Вовлечение синовиальных оболочек и сосудов, а затем и изменения костной ткани со всеми свойственными воспалению признаками деструкции делают процесс практически необратимым .
Первый признак АНГБК- боль, характеризующаяся неопределенной локализацией, и склонность к широкой иррадиации: в область поясницы и ягодицы, голени; в паховую область, а особенно часто (до 70% случаев) - в область коленного сустава. Именно эти отдаленные болевые ощущения воспринимаются как основные и легко уводят от правильного диагноза. При атипичной локализации боли возникает необходимость дифференцирования асептического некроза от пояснично-крестцового радикулита. Вначале боль малоинтенсивна, появляется при ходьбе, плохой погоде и исчезает в покое, постепенно становится постоянной и более интенсивной, усиливаясь при нагрузке. После периода обострений порой наступает облегчение, но затем симптомы заболевания нарастают. В ряде случаев начало заболевания может быть внезапным.
Во время осмотра, даже в ранние сроки заболевания, определяется заметная атрофия мышц бедра, а также уплощение ягодичных мышц на стороне поражения. По мере прогрессирования заболевания атрофия мышц нарастает, являясь чуть ли не патогномоничным синдромом, присущим АНКТ .
Одни из наиболее ранних симптомов заболевания - ограничения ротационных движений бедра, особенно внутренней ротации (80–85% случаев), сопровождающиеся болевым синдромом. Затем отмечается ограничение отведения, а в последнюю очередь - уменьшение подвижности в сагиттальной плоскости. Это объясняется тем, что на первых порах остеонекроз по существу является внесуставным заболеванием, поскольку патологический процесс локализуется в субхондральной зоне кости под толщей интактного суставного хряща, очень долго сохраняющего свою жизнеспособность, и таким образом обеспечивающего на длительный срок хорошую функцию сустава .
Весьма характерна для АНГБК его двусторонняя локализация (50–67% случаев). Зачастую патологический процесс, начавшись на одной стороне, в 90% случаев в течение 1 года возникает и на другой.
Преимущественное поражение у лиц мужского пола (80–90%) также можно использовать в качестве диагностического признака АНКТ.
Общее состояние у больных с асептическим некрозом не меняется, клинический анализ крови остается в норме.
Пионером лучевой диагностики является рентгенологический метод, который оказался универсальным способом исследования. Однако следует признать, что рентгенологический диагноз опаздывает, относительно предполагаемого клинического. Выявление начальных признаков патологических изменений в тазобедренных суставах является весьма сложной диагностической задачей. essay writing Важное значение в ранней диагностики поражения костей отводится радионуклидным методам. Сцинтиграфию широко используют для диагностики АНГБК. Аваскулярный участок в проксимальном эпифизе бедренной кости при АНГБК (так называемая зона ишемии) на сцинтиграммах проявляется снижением накопления радиофармпрепарата в зоне некроза с первых недель заболевания. С внедрением в клиническую практику компьютерной томографии появилась возможность по-новому, на более высоком уровне, оценить взаимоотношения костей, образующих тазобедренный сустав, качественно оценить плотность костной ткани головки бедренной кости.
Клиника и диагностика АНГБК на ранних стадиях трудны, при этом часто отмечаются диагностические ошибки. В большинстве же случаев пациенты лечатся по поводу «поясничного остеохондроза», «радикулита» или «ишиаса», «артроза» коленного сустава. Каждому третьему больному диагноз не устанавливается вовсе.
Диагностика АНГБК имеет ступенчатый характер. Наиболее консервативный метод - рентгенологический, в поддержку которого используют сцинтиграфию и другие методы исследования .
Лабораторные исследования пациентов свидетельствуют о нарушении капиллярного кровотока, повышенном внутрикостном давлении, синдроме гиперкоагуляции, нарушении вегетотрофической регуляции у этих больных.
Диагностика АНГБК состоит из двух этапов. На первом этапе при наличии жалоб на боль в области тазобедренного сустава, бедра и даже коленного сустава необходимо провести рентгенографию обоих тазобедренных суставов. На поздних стадиях асептического некроза этого исследования вполне достаточно. На рентгенограммах будет четко виден участок некроза, его форма и величина. Однако на ранних стадиях асептического некроза (даже в случае сильно выраженной phone spy for windows phone боли) на рентгенограммах тазобедренных суставов может не быть абсолютно никаких изменений. Поэтому в таких случаях обязательным является проведение специального исследования, называемого МРТ тазобедренных суставов. Только МРТ может выявить даже самый минимальный очаг АНГБК. Данное исследование является абсолютно безвредным и не использует рентгеновского излучения .
Выбор метода лечения при АНГБК, в первую очередь, зависит от стадии заболевания на момент установления диагноза. В настоящее время существует 5-стадийная характеристика патологических изменений. При первой стадии некроза рентгенологическое исследование не дает положительных результатов. Головка бедренной кости сохраняет присущую ей форму, костная структура также не изменена. При гистологическом же исследовании выявляется картина некроза губчатого вещества головки и ее костного мозга. Эту стадию некоторые авторы называют «дорентгеновской», «немой» или «теоретической» . Хотя второе определение неправомерно, поскольку клинически уже на этой стадии могут быть боль, ограничение движений в суставе, мышечная атрофия и др. Это свидетельствует о том, что отсутствие рентгенологических признаков заболевания не исключает наличия патологического процесса и требует дальнейшего исследования и динамического наблюдения. Вторая стадия импрессионного перелома характеризуется множеством микроскопических переломов на фоне патологических изменений (некротизированной) костной ткани. Рентгенологически на этой стадии головка бедренной кости гомогенно затемнена и нет структурного рисунка, высота ее по сравнению со здоровой стороной снижена, поверхность местами имеет вид уплотненных фасеток, суставная щель расширена. МРТ-исследование позволяет определить некротический дефект в головке бедренной кости. Третья стадия характеризуется как стадия рассасывания или «секвестрация». Головка еще более уплощается и состоит из отдельных бесструктурных изолированных фрагментов неправильной формы и величины, суставная щель еще более расширяется. Шейка бедренной кости укорочена и утолщена. В четвертой стадии, обозначенной как стадия репарации, происходит восстановление губчатого костного вещества головки. Рентгенологически секвестроподобные участки уже не видны, обрисовывается тень головки бедра, но структура кости еще не прослеживается, длительное время могут прослеживаться округлые кистовидные просветления. Наконец, пятая, конечная стадия (стадия вторичного деформирующего артроза) характеризуется рядом вторичных изменений по типу деформирующего артроза. Костная структура головки на этой стадии прослеживается, но форма ее значительно изменена, она уплощена, расширена в диаметре, поэтому суставная впадина ее не прикрывает, конгруэнтность суставных поверхностей нарушена. Видны краевые костные разрастания и вторичные дистрофические кисты.
Некоторые авторы придерживаются другого деления на стадии. Так, А.А. Корж и соавторы (1982) выделяют лишь 3 стадии процесса. Имеется деление заболевания на 6 и даже на 7 стадий.
Такое деление на стадии является относительным, поскольку процесс развивается динамически, одна стадия переходит в другую и не имеет строго очерченных границ. Тем не менее, с практической точки зрения такое деление необходимо. Каждая стадия характеризует степень и глубину патологического процесса, показывает, в каком направлении он развивается, то есть дает возможность прогнозировать в какой-то степени дальнейшее развитие процесса. В зависимости от этого и решается вопрос о тактике и выборе метода лечения. Обзорная рентгенография имеет относительное диагностическое значение на стадии деструкции структуры головки бедренной кости (особенно учитывая плохое качество снимков). В начальной стадии заболевания большое значение имеют клинические проявления и специальные методы исследования МРТ и компьютерная рентгеновская томография. Чувствительность МРТ-исследования достигает 90–100% в начальных стадиях заболевания.
Определенную диагностическую ценность имеют ультрасонография, радионуклидное исследования и лечебно-диагностическая пункция с измерением внутрикостного давления.
Основанием к проведению специальных методов исследования является боль в области тазобедренного сустава, особенно боль в паховой области с иррадиацией по бедренному нерву в область коленного сустава. Нередко патология тазобедренного сустава проявляется в виде нечеткой отраженной боли в коленном суставе. Особенное внимание следует обращать на пациентов, которые потенциально находятся в группах риска: мужчины в возрасте от 20 до 50 лет; лица, перенесшие травму или операцию тазобедренного сустава; пациенты с системными заболеваниями соединительной ткани (РА, СКВ, артериит); лица, apps to spy on someones phone длительно принимающие кортикостероиды; пациенты, злоупотребляющие алкоголем; лица с различными видами анемии; пациенты, имеющие патологию свертывающей системы крови; больные, получавшие радиационную или химиотерапию, а также с острым и хроническим панкреатитом.
ЛЕЧЕНИЕ
Лечение пациентов с АНГБК должно быть комплексным и дифференцированным в зависимости от стадии и клинического проявления заболевания, а прогноз заболевания зависит от ранней диагностики заболевания, распространенности остеонекроза и адекватной тактики лечения. Следует учитывать возможность двустороннего поражения тазобедренных суставов у большинства пациентов.
Медикаментозное лечение
В начальных стадиях заболевания патогенетически обоснованным является применение сосудистых препаратов для уменьшения ишемических изменений в головке беренной кости, нормализации реологических свойств крови, устранения микротромбозов. Такими свойствами обладает дипиридамол. Аналогичный эффект может быть получен при применении препаратов ксантинола никотината курсом 1–3 мес .
Регуляторы кальциевого обмена. Препараты этидроновой кислоты способствуют ремоделированию нормальной костной ткани в сочетании с альфакальцидолом и препаратами кальция (из расчета 1,5 г/сут). Курс лечения - 8 мес .
Хондропротекторы - препараты, восстанавливающие метаболизм суставного хряща в сочетании с витаминами группы В (В 6 , В 12) - применяются курсами 1–2 раза в год.
Хирургическое лечение
Несмотря на успехи хирургического лечения (чрезвертельная ротационная остеотомия, предупреждающая коллапс головки бедренной кости в 95% случаях, субхондральная аутопластика головки бедра), АНГБК является прежде всего проблемой амбулаторной ортопедии . К сожалению, полное восстановление сустава, как правило, не наступает, однако в большинстве случаев возможно достижение вполне приемлемого исхода заболевания: предотвращение поражения контралатерального сустава; уменьшение деструктивных процессов в головке бедра и вторичного коксартроза; порочных установок бедра в положении сгибания, приведения и избыточной ротации; минимального ограничения объема движений в тазобедренном суставе; хорошего функционального состояния мышц и нерезко выраженного болевого синдрома.
Важное место в комплексном лечении АНГБК занимают реабилитационные мероприятия, что в последующем улучшает качество жизни пациентов.
Список использованной литературы
1. Атманский И.А.
(2006) Клинико-биомеханическое обоснование реконструктивно-восстановительных вмешательств help me write a essay на бедренной кости при патологии тазобедренного сустава: Дис. … д-ра мед. наук. Курган, 395 с.
2. Ахтямов И.Ф., Коваленко А.Н., Юосеф А.И. и др.
(2006) Многоочаговый асептический некроз костей. Казан. мед. журн., 3: 171–174.
3. Берглезов М.А., Андреева Т.М.
(2006) Остеоартроз (этиология, патогенез). Вестн. травматол. ортопед., 4: 79–87.
4. Диваков М.Г.
(1990) Идиопатический асептический некроз головки. Совр. мед., 8: 92–96.
5. Зоря В.И.
(1994) Возможные причины асептического некроза головки бедренной кости у взрослых и вопросы его диагностики. Травматол. ортопед. России, 5: 46–53.
6. Ибатуллин И.А.
(2000) Гомеостаз и артериальная гипертезия. Сегментарное строение лимфатической системы и его клиническое значение: Руковод. для врачей. - 2-е издание, Медицина, Казань, 308 с.
7. Кильчевский Г.С.
(1963) Аваскулярные некрозы головки бедренной кости в эксперименте. Ортопед., травматол., 7: 30–34.
8. Корж А.А.
(1989) Керамические имплантанты при хирургическом лечении асептического некроза головки бедренной кости. Ортопед, травматол., 10: 1–3.
9. Коробков А.Я.
(1994) Асептический некроз головки бедренной кости у взрослых. Этиология и патогенез. Травматол. ортопед. России, 6: 111–119.
10. Митбрейт И.М., Голубенко Г.Н.
(2000) Асептический некроз головки бедренной кости у взрослых. Этиология, патогенез, выбор метода лечения: Сб. науч. тр. к 60-летию ГКБ № 13 «Актуальные вопросы практической медицины», РГМУ, Москва, с. 366–368.
11. Насонов Е.Л., Насонова В.А.
(ред.)
(2010) Национальное руководство. Ревматология, с.101–105.
12. Насонов E.Л.
(2002) Фармакотерапия ревматоидного артрита с точки зрения доказательной медицины: новые рекомендации. РМЖ, 6: 11–23.
13. Рейнберг С.А.
(1964) Рентгенодиагностика заболеваний костей и суставов. Т. 2. Медицина, Москва, 372 с.
14. Agarwala S.
(2005) Efficacy of alendronate, a bisphosphonate, in the treatment of AVN of the hip. A prospective open-label study. Rheumatology (Oxford). 44(3): 352–359.
15. Aldridge J.M.
(2004) Free vascularized fibular grafting for the treatment of postcollapse osteonecrosis of the femoral head. Surgical technique. J. Bone Joint Surg. Am., 86-A(Suppl. 1): 87–101.
16. Assouline-Dayan Y.
(2002) Pathogenesis and natural history of osteonecrosis. Semin Arthritis Rheum., 32(2): 94–124.
17. Babis G.C., Sakellariou V., Parvizi J. et al.
(2011) Osteonecrosis of the femoral head. Orthopedics, 34(1): 39.
18. Bluemke D.A., Petri M., Zerhouni E.A.
(1995) Femoral head perfusion and composition: MR imaging and spectroscopic evaluation of patients with systemic lupus erythematosus and at risk for avascular necrosis. Radiology, 197(2): 433–438.
19. Ito H.
(2007) Health-related quality of life in patients with systemic lupus erythematosus after medium to long-term follow-up of hip arthroplasty. Lupus, 16(5): 318–323.
20. Kawate K.
(2007) Indications for free vascularized fibular grafting for the treatment of osteonecrosis of the femoral head. BMC Musculoskelet. Disord., 8: 78.
21. Pritchett J.W.
(2001) Statin therapy decreases the risk of osteonecrosis in patients receiving steroids. Clin. Orthop. Relat. Res. 386: 173–178.
22. Slavkovic S.
(2005) Idiopathic avascular necrosis of the femoral head in adolescents - diagnostics and management. Acta Chir. Iugosl., 52(2): 43–48.
АСЕПТИЧНИЙ НЕКРОЗ КІСТКОВОЇ ТКАНИНИ В РЕВМАТОЛОГІЇ
Г.О. Проценко
Резюме. В оглядовій статті наведено дані вивчення складної проблеми в ревматологічній практиці - асептичного некрозу кісткової тканини. Недостатня поінформованість практичних лікарів щодо цієї патології, прихований, поступовий перебіг захворювання, відсутність чітких патогномонічних симптомів, особливості больового синдрому, тривале збереження рухливості в суглобі, що складають враження клінічного благополуччя, потребують подальшого вивчення цієї проблеми.
Ключові слова: асептичний некроз кісткової тканини, діагностика, лікування.
Avascular bone tissue necrosis in rheumatology
G.O. Protsenko
Summary. The recent scientific data about avascular bone necrosis in rheumatology are presented in the article. Incomplete knowledge of this problem by physicians, latent course of the disease, the absence of direct specific symptoms, pain syndrome peculiarities, long functional joint capacity, which create an impression of clinical prosperity, make the research of the condition actual.
Key words: avascular bone tissue necrosis, diagnostics, treatment.
Адреса для листування:
Проценко Галина Олександрівна
03680, Київ, вул. Народного ополчення, 5
ННЦ «Інститут кардіології ім. М.Д. Стражеска» НАМН України
Ранее выявление аваскулярных повреждений кости является актуальным вопросом лучевой диагностики.Одной из излюбленных локализаций аваскулярного некроза является таранная кость. При повреждениях голеностопного сустава в 6,5% случаев возникает аваскулярный некроз в блоке таранной кости. Среди всех субхондральных повреждений блок таранной кости поражается в 4% случаев. Однако на ранней стадии это заболевание диагностируется редко, так как зачастую скрывается под маской других заболеваний, а , наиболее часто используемая при травмах голеностопного сустава, не позволяет выявить его ранние признаки.
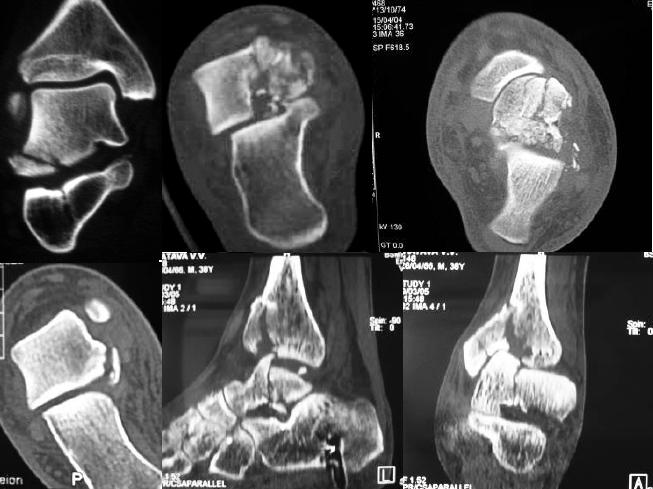
Обследовано 85 пациентов с различными травма- тическими повреждениями голеностопного сустава в возрасте от 17 лет до 61 года.Исследование проводили на SIEMENS Magnetom Symphony 1.5 T c использованием T1-взвешенных изображений в аксиальной плоскости, T2-взвешенных изображений в аксиальной и фронтальной плоскостях с подавлением сигнала жировой ткани, T2-взвешенных 3D изображениях в сагиттальной плоскости.Всем пациентам также была проведена сравнительная рентгенография голеностопного сустава в прямой проекции.
Для оценки результатов МРТ-исследований применяют классификацию стадий субхондральных изменений в таранной кости, предложенную D. W. Stoller (1997) или S. Нepple (1999).
Все пациенты жаловались на упорные боли, усиливающиеся при нагрузке, скованность, рецидивирующий отек сустава. Из 85 обследованных пациентов с патологией голеностопного сустава, аваскулярный некроз, исходя из Бристольской классификации, был выявлен у тринадцати больных (15,3%). Давность травмы у пациентов с выявленным аваскулярным некрозом в сроки от 6 до 12 месяцев и в срок более года составила 38,45%, в срок до 3 месяцев 15,4%, от 3 до 6 месяцев — 7,7%.
Два пациента были направлены для в связи с исходом изолированных повреждений связочного аппарата, у шести пациентов (46%) были последствия переломов костей голено- стопного сустава и повреждений связочного аппарата, у трех человек (23%) наблюдали посттравматический деформирующий остеоартроз и двух человек (15,5 %) были клинические проявления хронической посттравматической нестабильности в голеностопном суставе.
По мнению П. Л. Жаркова (1996), дегенеративно- дистрофическое поражение суставов с кистовидной перестройкой сочленяющихся костей и асептический остеонекроз являются различными проявлениями поражения патологическим процессом суставных концов сочленяющихся костей. Клинически эти формы сходны и отличаются лишь по проявлениям. При асептическом некрозе в первой фазе определяется участок уплотнения клиновидной или сегментарной формы с нечеткими контурами в суставной головке. Уплотнение обусловлено эндостальным костеобразованием в зоне концентрации напряжения. Во второй фазе отмечается ограничение участка уплотнения зоной остеолиза и реактивного склероза вследствие развития повторных ишемических нарушений. Третья фаза характеризуется инконгруэнтностью суставных поверхностей за счет продавливания уплотненного участка в толщу кости, реже наблюдается его выстояние в полость сустава. В четвертой фазе к описанным изменениям присоединяется нерезкое неравномерное сужение суставной щели и краевые костные разрастания на суставной головке. В пятой фазе изменения суставного хряща нарастают, что выражается еще большим сужением суставной щели и краевыми костными разрастаниями не только на головке, но и на впадине, т. е. к одной форме дегенеративно-дистрофического поражения (асептическому остеонекрозу) присоединяется другая - деформирующий артроз. И. А. Пахомов (2008) среди пациентов с заболеваниями и повреждениями стопы и голеностопного сустава выделяет группу больных с асептическим некрозом таранной кости (болезнью Муше) - спонтанно возникающим и быстро прогрессирующим процессом дегенерации голеностопного сустава с исходом в деформирующий артроз. Как свидетельствуют данные, довольно часто причиной асептического некроза блока таранной кости является травма, морфологические проявления которой не всегда характеризуются наличием перелома, а обусловлены повреждением мягких тканей. Поскольку невыявленный асептический некроз таранной кости приводит к деформирующему артрозу голеностопного сустава, тяжелому, длительно протекающему заболеванию, в ряде случаев заканчивающемуся артродезом голеностопного сустава, ранняя диагностика всех составляющих патологического комплекса при болевом синдроме в области голеностопного сустава является чрезвычайно важной. Результаты работы показали, что
